OSTALI SEMINARSKI RADOVI
IZ HEMIJE: |
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
Polietilen i polipropilen, PVC, Polistiren i Teflon, Najloni, termostabilne plastične mase
1. Polietilen i polipropilen
Polietilen
U zavisnisti od katalizatora koji s koristi u polimerizaciji razlikujemo
dva tipa polietilena:
- polietilen velike gustine HDPE
- polietilen male gustine LDPE
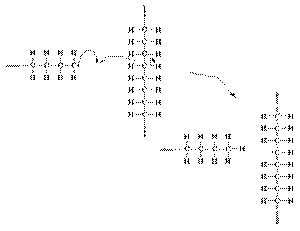 Mehanizam
nastajanja racvastog polietilena
Mehanizam
nastajanja racvastog polietilena
U jednom momentu nespareni elektron na kraju polimernog lanca može raskinuti
vezu C-H u drugom polimernom lancu i na taj način stvoriti radikal u samom
polimernom lancu. Tako dolazi do račvanja na lancu jer nastali radikal
dalje reaguje sa molekulima etena i dobijaju se račvasti polietileni male
gustine.
Polietilen visoke gustine dobija se koordinacionom polimerizacijom (Ziegler-Nattan-ovi
katalizatori).
 Primenom
metalocenskih katalizatora može se dobiti polietilen molekulske mase od
tri do šest miliona od koga se izrađuju vlakna izuzetne jačine.
Primenom
metalocenskih katalizatora može se dobiti polietilen molekulske mase od
tri do šest miliona od koga se izrađuju vlakna izuzetne jačine.
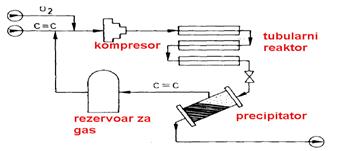
Polietilen niske gustine se dobija u tubularnim reaktorima na temperaturi
od 150 do 300 ° C i pritisku od 2000 do 3000 atmosfera.
Polietilen visoke gustine se dobija na pritisku od 2 do 10 atmosfera u
reaktorima sa mešanjem. Kao katalizatori se koriste trietilaluminijum
i titantetrahlorid.
Polietilen se primenjuje za izradu ambalaže, vodovodnih cevi i drugo.
Polietilen niske gustine se koristi kaom folija i za nanošenje folije
na karton i papir.
Polipropilen

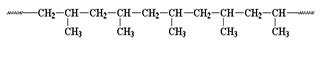 Primenom
Ziegler-Nattan-ovog katalizatora moguće je dobiti izotaktički polimer
kod koga su sve metil grupe sa iste strane. Polipropilen ima višu tačku
topljenja od polietilena visoke gustine (oko 160 ° C).
Primenom
Ziegler-Nattan-ovog katalizatora moguće je dobiti izotaktički polimer
kod koga su sve metil grupe sa iste strane. Polipropilen ima višu tačku
topljenja od polietilena visoke gustine (oko 160 ° C).
Usled račvanja na polimernom lancu nastaje tercijarni vodonikov atom koji
je osetljiv na oksidaciju. Ovaj problem se u prime3ni prevsazilazi dodatkom
fenolnih antioksidanasa polimeru. Pored toga metil grupa ukrućuje polimer
što dovodi do njegove krtosti na niskim temperaturama. Ovaj problem se
prevazilazi dodatkom etilen-propilen-dienskog polimera.
Polipropilen se koristi za izradu sintetskih tepiha (na bazenima), za
izradu posuda za hranu (može se prati u mašinama za sudove za razliku
od polietilena).
2. PVC, Polistiren i Teflon
Polistiren

Polistiren se uglavnom dobija polimerizacijom u masi. Reakcija se inicira
peroksidima i toplotom. Temperatura se podešava tako da masa stalno bude
u istopljenom stanju. Dodatkom 10 % pentana i zagrevanjem dobija se ekspandovana
masa (stiropor).
Nedostatak polistirena je njegova krtost i omekšavanje u vrućoj vodi.
Ovo se može prevazići dodatkom 10 % gume (polibutadien) u stirenski monomer
pre polimerizacije. Na ovaj način se znatno poboljšavaju njegove mehaničke
osobine. Povećana otpornost na toplotu se postiže kopolimerizacijom sa
akrilonitrilom (15 do 30 % akrilonitrila. Kombinacija ova dva efekta se
postiže u akrilonitril-butadien-stirenskom polimeru. Ovakav polimer pokazuje
odlične osobine i primenjuje se za branike na automobilima, delove gume
kod automobila, elektronske kabinete, uređaje i drugo.
PVC
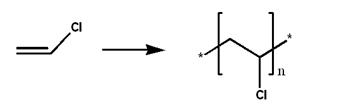 Polivinilhlorid
je treći po proizvodnji iza polietile-na i polipropilena. Polimizuje se
suspenzionom polimerizacijom iniciranom peroksidima. Manji deo se polimerizuje
emulzionom polimerizacijom. Da bi se lakše oblikovao polimerizacija se
vrši na 40 do 55 ° C i onda se polimer meša sa 20 do 80 delova na sto
dioktilftalata kao plastifikatora.
Polivinilhlorid
je treći po proizvodnji iza polietile-na i polipropilena. Polimizuje se
suspenzionom polimerizacijom iniciranom peroksidima. Manji deo se polimerizuje
emulzionom polimerizacijom. Da bi se lakše oblikovao polimerizacija se
vrši na 40 do 55 ° C i onda se polimer meša sa 20 do 80 delova na sto
dioktilftalata kao plastifikatora.
Pored toga PVC-u se dodaju i ostali aditivi kao stabilizatori, sredstva
za samogasivost, antioksidansi i drugo.
Koristi se kao izolator, za izradu kanalizacionih cevi, plastične prozore
i vrata a nekada se koristio za izradu gramfonskih ploča.
Teflon
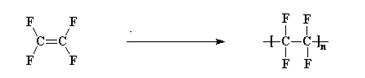 Teflon
je zaštićeno ime za politetrafluoroetilen. Polimer se dobija slobodno
radikalskom polimerizacijom. Ovaj polimer pokazuje odlične osobine u primeni.
Poseban značaj je za izradu sudova pošto se teflon topi tek na 327 ° C.
Prednost teflona u odnosu na ostale materijale je što za njega ništa ne
prianja.
Teflon
je zaštićeno ime za politetrafluoroetilen. Polimer se dobija slobodno
radikalskom polimerizacijom. Ovaj polimer pokazuje odlične osobine u primeni.
Poseban značaj je za izradu sudova pošto se teflon topi tek na 327 ° C.
Prednost teflona u odnosu na ostale materijale je što za njega ništa ne
prianja.
Ova osobina teflona se objašnjava velikim brojem atoma fluora koji je
najelektronegativniji elemenat. Elektroni oko fluora stvaraju štit oko
polimera i sprečavaju hemijska jedinjenja da priđu polimeru. Pored toga
vrlo jaka veza C-F čini teflon inertnim te se koristi u hemijskoj industriji.
Medjutim, njegova nereaktivnost ga čini problematičnim za primenu jer
je problem naneti ga na površinu. Nanošenje se bazira uglavnom na mehaničkim
interakcijama.
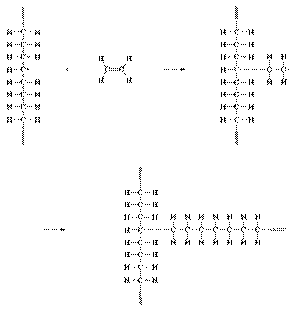
3. Najloni
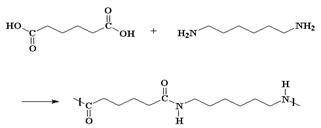 Najlon
je zajednički naziv za polimere nastale polimerizacijom diamina i dikarbonske
kiseline ili polimerizacijom amino kiselina. Najpoznatiji predstavnik
je najlon 6,6 koji nastaje polimeri-zacijom adipinske kiseline i heksametilen
diamina.
Najlon
je zajednički naziv za polimere nastale polimerizacijom diamina i dikarbonske
kiseline ili polimerizacijom amino kiselina. Najpoznatiji predstavnik
je najlon 6,6 koji nastaje polimeri-zacijom adipinske kiseline i heksametilen
diamina.
Prvi broj iza najlona označava broj C atoma u diaminu dok drugi broj označava
broj C atoma u kiselini. Tako su pored najlona 6,6 u primeni i najloni
6,10 i najlon 6,12. Mešanjem kiseline i diamina u rastvoru pada amonijum
so kiseline. Nakon toga so se polimerizuje na 280 ° C pod pritiskom u
autoklavu uz mešanje. Nakon toga stopljeni najlon se prebacuje u mašinu
za izvlačenje vlakana. Najlon se boji u fazi polimerizacije.
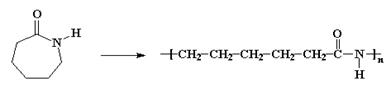 Najlon
6 poznatiji pod nazivom Perlon dobija se polimerizacijom kaprolaktama.
Polimerizacija može biti termalna ili anjonska pri čemu dolazi do otvaranja
prstena i reakcije amino kiseline sa sledećim molekulom kaprolaktama.
Pored najlona 6 poznat je i najlon 12.
Najlon
6 poznatiji pod nazivom Perlon dobija se polimerizacijom kaprolaktama.
Polimerizacija može biti termalna ili anjonska pri čemu dolazi do otvaranja
prstena i reakcije amino kiseline sa sledećim molekulom kaprolaktama.
Pored najlona 6 poznat je i najlon 12.
4. Termostabilne plasticne mase
Fenol-formaldehidne smole 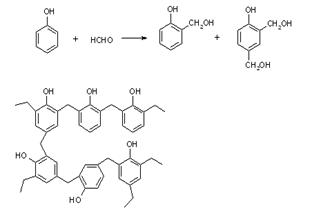 Polimerizacija
fenol-formaldehidne smole sastoji se iz tri faze:
Polimerizacija
fenol-formaldehidne smole sastoji se iz tri faze:
- u prvoj fazi nastaju niskomolekularni oligomeri koji su rastvorni i reaktivni
- u drugoj fazi nastaje polimer koji je još uvek topljiv i reaktivan
- izlivanjem smole u kalupe pod pritiskom i zagrevanjem dolazi do umrežavanja i nastaje termostabilni polimer
Glavna primena je kao adheziv u fabrikaciji iverice, laminata i kompozita
Kopolimerizuju sa celulozom
P-CH2OH + HO-celuloza P-CH2-O-celuloza
preuzmi
seminarski rad u wordu » » »
