OSTALI SEMINARSKI RADOVI
IZ HEMIJE: |
|||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||
Katalaza
Građa, osobine i uloga
Katalaza je čest enzim koji se nalazi u skoro
svim živim bićima koji su izloženi kiseoniku, gde ima funkciju da katalizuje
raspad vodonik peroksida na vodu i kiseonik. Katalaza je jedan od “najjačih“
enzima; jedan enzim katalaze može da dekompozira 40 miliona molekula vodonik
peroksida u vodu i kiseonik za jednu sekundu.
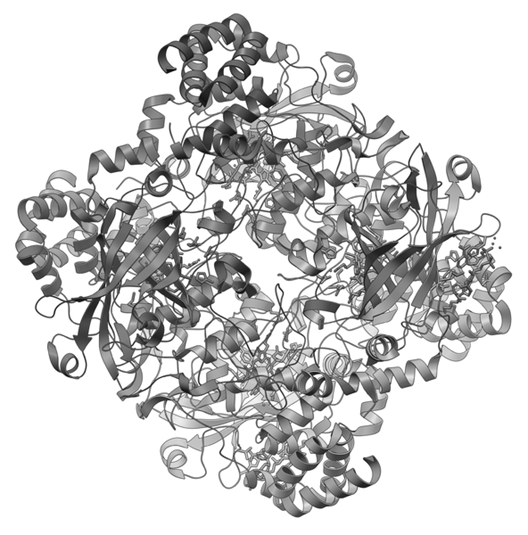
Katalaza je tetramer što znači da se sastoji iz četiri podjedinice, od
kojih svaka se sastoji od preko 500 amino kiselina. Sadrži četiri porfirina
hema, grupa koje omogućavaju da enzim reaguje sa vodonik peroksidom. Porfinir
hema je heterociklični prsten u čijem središtu se nalazi atom gvožđa.
Optimalna vrednost pH za ljudsku katalazu se kreće oko 7, i ima prilično
širok maksimum (učinak reakcije se ne menja primetno za pH između 6.8
i 7.5). Optimalna pH za katalaze drugih organizama varira između 4 i 11
u zavisnosti od vrsta. Optimalna temperature takođe varira od vrste do
vrste a za čoveka iznosi oko trideset i sedam stepeni Celzijusa(37°C).
S druge strane Arheje, prabakterije, imaju katalazu koja ima za optimalnu
temperaturu 90°C.
Katalaza test
Katalaza test je jedan od tri glavna testa koji koriste
mikrobiolozi radi identifikacije vrsta bakterija. Izolovano prisustvo
enzima katalaze u testu se otkriva korišćenjem vodonik peroksida. Ako
bakterija poseduje katalazu(tj. ako je katalaza-pozitivna), onda kada
se mala količina izolovane bakterije doda u vodonik perosid, mehurići
kiseonika se zapažaju.
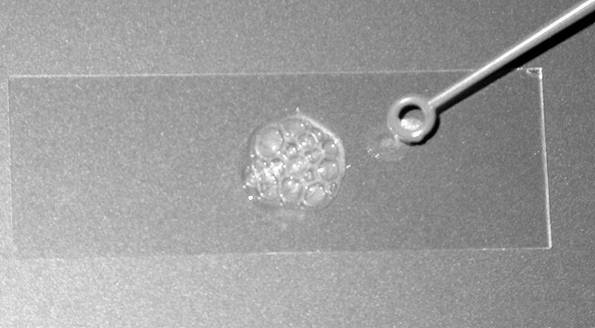
U mikrobiologiji, katalaza test se koristi radi razlikovanja bakterijskih
vrsta u laboratoriji. Test se vrši stavljanjem kapljice vodonik peroksida
na mikroskopsko staklo. Korišćenjem odgovarajućeg štapića, naučnik postavlja
koloniju bakterija na kapljicu vodonik peroksida.
Ako se formiraju mehurići, organizam je katalaza-pozitivan. Stafilokoke
i Mikrokoke su katalaza-pozitivne. Drugi katalaza-pozitivni organizmi
uključuju Listeriju, Burkolderia cepaciju, Ešerihiju koli i Salmonelu.
Ako se mehurići ne formiraju organizmi su katalaza-negativni. Streptokoke
i Enterokoke su katalaza-negativne.
Dok sam katalaza test ne može da identifikuje poseban organizam, u kombinaciji
sa drugim testovima poput otpora na antibiotik,on može pomoći u postavljanju
dijagnoze.
Istorija
Katalaza je prvi put primećena kao supstanca 1818. kada
je Luis Dzek Tenard, koji je otkrio H2O2 (vodonik peroksid), sugeriosao
da je njegov raspad uzrokovan sustancom. 1900. Oskar Lui je bio prvi koji
joj dao ime katalaza, i pronašao je njeno prisustvo u mnogim biljkama
i životinjama. 1937. Dzejms B. Samner je kristalizovao katalazu iz goveđe
jetre i 1938. se došlo do težine molekula.
1969. se otkrio lanac amino kiselina koje izgrađuju goveđu katalazu. Potom
se 1981. obelodanila 3D struktura ovog proteina.
Reakcija
Reakcija razlaganja vodonik peroksida na vodu i kiseonik u kojoj učestruje katalaza:
2H2O2 → 2H2O + O2
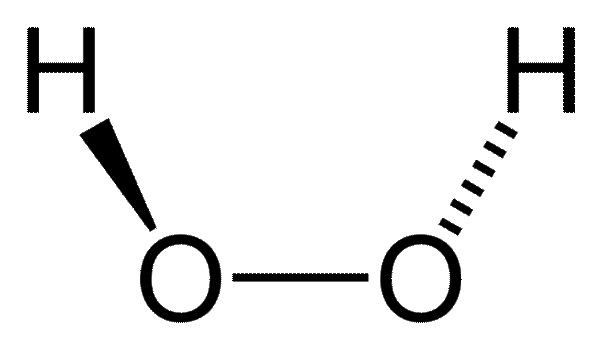
Vodonik peroksid
Iako se u celosti mehanizam rada katalaze ne zna, veruje
se da se on odvija u dva stupnja:
H2O2 + Fe(III)-E → H2O + O=Fe(IV)-E(.+)
H2O2 + O=Fe(IV)-E(.+) → H2O + Fe(III)-E + O2
Ovde Fe()-E predstavlja gvožđe u centru hema, sastavnog dela katalaze.
Fe(IV)-E(.+) je mezomerična forma Fe(V)-E, što znači da gvožđe nije u
potpunostioksidovano do +V ali je primio “pomoćne elektrone”
od liganda hema. Ovaj hem mora biti izvučen kao radikalni katjon (.+).
Kada vodonik peroksid dođe do aktivacionog centra on reakguje sa amino
kiselinom Asn147 (asparagin na poziciji 147) i His74 (histidin na poziciji
74), uzrokuje da se proton (vodonikov jon) prebaci između atoma kiseonika.
Slobodni atom kiseonika odlazi, oslobađajući novooformljeni molekul vode
i Fe(IV)=O. Fe(IV)=O reaguje sa drugim vodonik peroksidom i ponovo formira
Fe(III)-E proizodeći vodu i kiseonik. Reaktivnost centralnog atoma gvožđa
može biti poboljšana prisustvom fenolnog liganta Tyr357 u petom ligandu
gvožđa, koji može da pomogne u oksidaciji Fe(III) u Fe(IV). Efikasnost
reakcije se takođe može poboljšati interakcijom His74 i Asp147 sa reakcionim
intermediumom. Generalno, efikasnost se može izračunati Mihaelis-Menteninom
jednačinom.
Katalaza takođe može oksidovati razne otrove, kao sto su formaldehid,
mravlja kiselina, fenoli i alkoholi. Ona to radi koristeći vodonik peroksid
prema narednoj reakciji:
H2O2 + H2R → 2H2O + R
Još jednom, potpuni mehanizam reakcije je nepoznat.
Bilo koji jon teškog metala (kao katjon bakra u bakar(II) sulfatu) će
se ponašati kao nekonkurentan inhibitor katalaze (smanjiće aktivnost enzima
katalaze). S druge strane, otrovni cijanid je konkurentan inhibitor katalaze,
čvrsto se vezujući za hem katalaze on u potpunosti prekida reakciju enzima.
Ćelijska uloga
Kod čoveka i drugi enzimi poput glutation peroksidaze razlažu
vodonik peroksid. Glutation peroksidaza je u fiziološkim uslovima (mala
koncentracija vodonik peroksida), čak i aktivniji od katalaze. Kad koncentracija
vodonik peroksida poraste uključuje se katalaza. Kod čoveka je široko
zastupljena u ćelijama jetre u peroksizomima i u eritrocitima (crvenim
krvnim zrncima).
Vodonik peroksid je štetan nus produkt mnogih normalnih metaboličkih procesa:
da bi se sprečila oštećenja on mora biti brzo pretvoren u neke druge,
manje opasne supstance. Stoga ćelije često koriste katalazu da brzo razlože
vodonik peroksid na manje reaktivan gas O2 i molekul vode.
Pravi biološki značaj katalaze još uvek nije poznat: Miševi koji imaju
manjak katalaze su fenotipski normalni. Nedostatak katalaze može povećati
izgled za dobijanje Dijabetesa Tip II.
Katalaza se obično nalazi u ćeliskoj organeli zvanoj peroksizom. Peroksizomi
u ćelijama biljaka su uključeni u proces fotorespiracije (korišćenje kiseonika
i produkcija ugljen dioksida) i simbiotičke fiksacije azota (razaranje
dvoatomskog molekula (N2) radi dobijanja atoma azota). Vodonik peroksid
se koristi kao antimikrobno sredstvo kada su ćelije inficirane patogenom.
Patogeni koji su katalaza-pozitivni, kao što su Mikrobakterijum tuberkulozis,
Legionela pheumofila i Kampilobakter jejunin, proizvode katalazu da bi
deaktivirale radikale peroksida, time omogućavaju sebi da prežive nepovređene
unutar domaćina.
Raspodela među organizmima
Sve znane životinje koriste katalazu u svakom organu, sa naročito izraženom
koncentracijom u jetri.
Katalaza je univerzalna i među biljkama. Mnoge gljive takođe proizvode
ovaj enzim u velikim količinama.
Jako je malo poznatih aerobnih mikroorganizama koji ne koriste katalazu.
Katalaza je nađena i u anaerobnim mikroorganizmima kao što je Metanosarkina
barkeri.
Primena
Katalaza se primenjuje u industriji hrane za uklanjanje
vodonik peroksida iz mleka pre proizvodnje sira. Još jedna primena kod
hrane je omot gde sprečava hranu od oksidacije. Katalaza se takođe koristi
u tekstilnoj industriji za uklanjanje vodonik peroksida iz tkanina osiguravajući
da je materijal bezbedan.
Slabija, i znatno manja, upotreba je u higijeni očnih sočiva – mali broj
produkata za čišćenje sočiva koristi vodonik peroksid kao rešenje. Potom
se rastvor koji sadrži katalazu koristi da razloži vodonik peroksid pre
ponovne upotrebe.
U skorije vreme katalaza se počela koristiti u industriji tretmana i nege
lica. Tretmani maska kombinuju enzim sa vodonik peroksidom na licu radi
povećavanja ćelijskog disanja gornjih slojeva epidermisa.
Sedenje kose
Prema skorašnjim naučnim studijama, nizak nivo katalaze može imati ulogu u procesu sedenja ljudske kose. Vodonik peroksid prirodno proizvodi telo a katalaza razlaže. Ako postoji pad u nivou katalaze, vodonik peroksid ne može biti razoren, Ovo uzrokuje da vodonik peroksid izbeljuje kosu od iznutra ka spolja. Naučnici veruju da ovo otkriće može jednog dana pomoći tretmanima protiv sedenja kose starijih ljudi.
Uloga kod bolesti
Peroksizomalan poremećaj ili akatalazija nastaje zbog nedostatka katalaze i same njene funkcije. Dovodi do oboljenja desni, nekad i gangrene. Ova bolest je relativno česta kod Japanaca i Koreanaca. Ponekad dolazi do genetskih izmena u izgledu i aktivnosti katalaze koji su povezani sa oksidacionim oštećenjima DNK i to dovodi do povećanog individualnog rizika od raka.
Literatura:
www.wikipedia.com
preuzmi
seminarski rad u wordu » » »
